МОЯ ТВОРЧЕСКАЯ ЛАБОРАТОРИЯ






 "Каждая
цивилизация в определенном возрасте имеет возможность возвысить, или
разрушить себя. Если делается выбор в пользу возвышения, то возникает
импульс, позволяющий появиться учениям об утерянных законах сущего". (Высший
разум, ченнелинг).
М.И. Беляев, 2015г,©
"Каждая
цивилизация в определенном возрасте имеет возможность возвысить, или
разрушить себя. Если делается выбор в пользу возвышения, то возникает
импульс, позволяющий появиться учениям об утерянных законах сущего". (Высший
разум, ченнелинг).
М.И. Беляев, 2015г,©
|
Таким образом, атомы и ионы химических элементов при формировании минералов неорганической природы способны плотно упаковываться в кристаллическую решетку определенного типа в зависимости от их размеров и видов химической связи. Форма геометрического узора, который получается при этом (цепочечный, слоистый, каркасный и др.), определяет и морфологию образующихся кристаллов (рис. 8). Форма кристаллов определяется их поверхностными гранями. Геометрическое расположение граней определяется законом Бравэ: при образовании кристаллов развитие и частота появления граней, ограничивающих кристалл, зависят от густоты расположения атомов и ионов на этих гранях (ретикулярная плотность). Чем гуще грани покрыты атомами, тем они важнее, т. е. чаще встречаются на кристаллах. 16 В зависимости от плотности распределения атомов и ионов в кристаллической решетке происходит рост кристаллов той или иной формы. Из любых возможных направлений в кристаллической решетке наиболее конкурентоспособными поверхностями роста являются те, где атомы ближе расположены друг к другу, так как здесь меньше расстояние между ними и поэтому они способны более прочно связываться друг с другом, отсекая все другие направления. Но это еще не значит, что та или иная плоскость с высокой плотностью атомов будет быстрее расти. Даже совсем наоборот: согласно закону Бравэ грани кристалла растут со скоростью, обратно пропорциональной плотностям их распределения. Это понятно, ведь, например, при одинаковой концентрации в растворе грани с большей плотностью атомов больше их поглощают из раствора и этим быстрее снижается их концентрация около этой грани, что ведет к замедлению ее пространственного продвижения. Но именно эти медленно растущие грани и определяют в конечном счете основные черты конфигурации кристаллов, так как быстро растущие грани зарастаются ими (рис. 9). Представляется интересным обратить внимание на механизмы роста кристаллов. Атомы, молекулы и ионы, составляющие газообразные или жидкие (растворы и расплавы) вещества, находятся в непрерывном движении. Они постоянно сталкиваются друг с другом, и периодически это столкновение ведет к образованию зародышей - микроскопических фрагментов будущей структуры. Чаще всего такие зародыши распадаются, что связано либо с собственными колебаниями, либо с бомбардировкой их свободными частицами. Для начала кристаллизации нужно, чтобы зародыш достиг критической величины, т. е. содержал такое количество частиц, при котором присоединение следующей частицы сделало бы разрастание зародыша более энергетически выгодным, чем его распад. Такая возможность для большинства веществ появляется либо с понижением температуры, в результате чего уменьшаются тепловые колебания, либо с повышением концентрации вещества в растворе или газе, что приводит к увеличению вероятности встречи частиц друг с другом, т. е. возникновению зародышей. Причем кристаллизация протекает не во всем объеме, а преимущественно там, где возникнут зародыши.  17 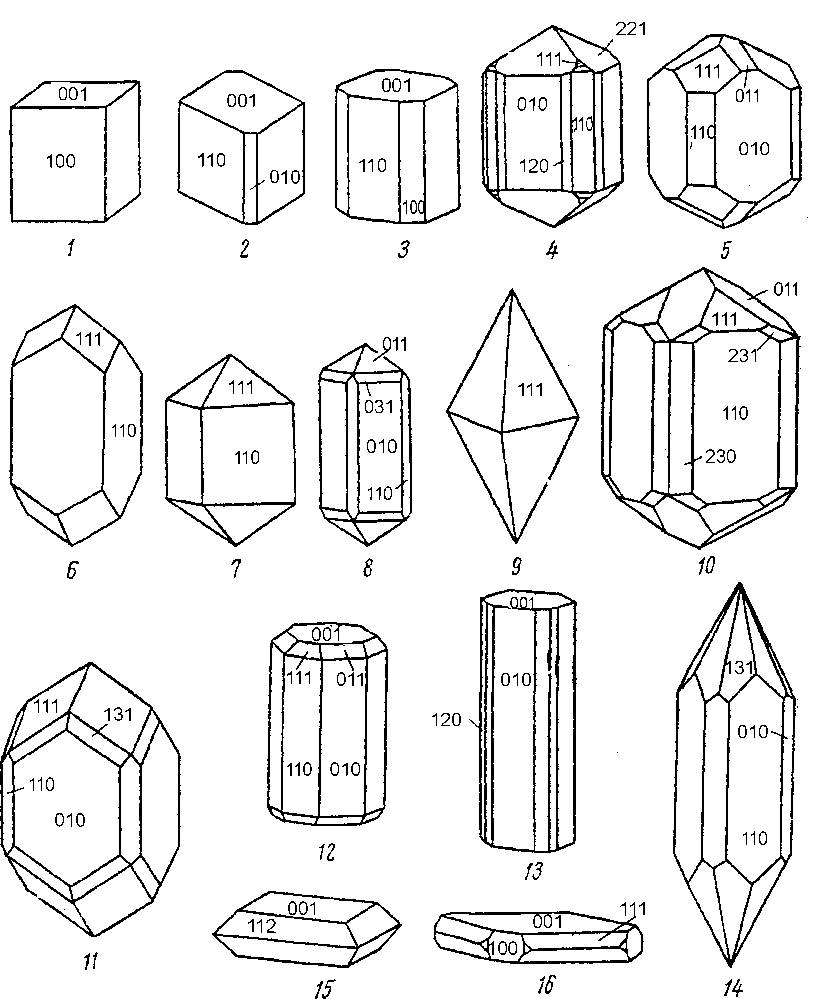 Рис. 8. Габитусные типы кристаллов тетрагональной сингонии 1 - мелилит Са2(М§,А1)[(81,А1)2 8107); 2 - скаполит (Ка,Са)4(С1,С03)[А1(8і,А1)8і208]; 3 - висмутит Ві202[С03]; 4 - селаит МеБ2; 57, 12 - касситерит 8п02; 6, 14 - циркон 2г[8104]; 8 - ксенотим У[Р04]; 9 -анатаз Т102; 10 - рутил Т102; 11 - торит ТЬ[8104]; 13, 16 - апофиллит Кса[8і4010]2Р-8И20; 15 - шеелит Са[\У04] |